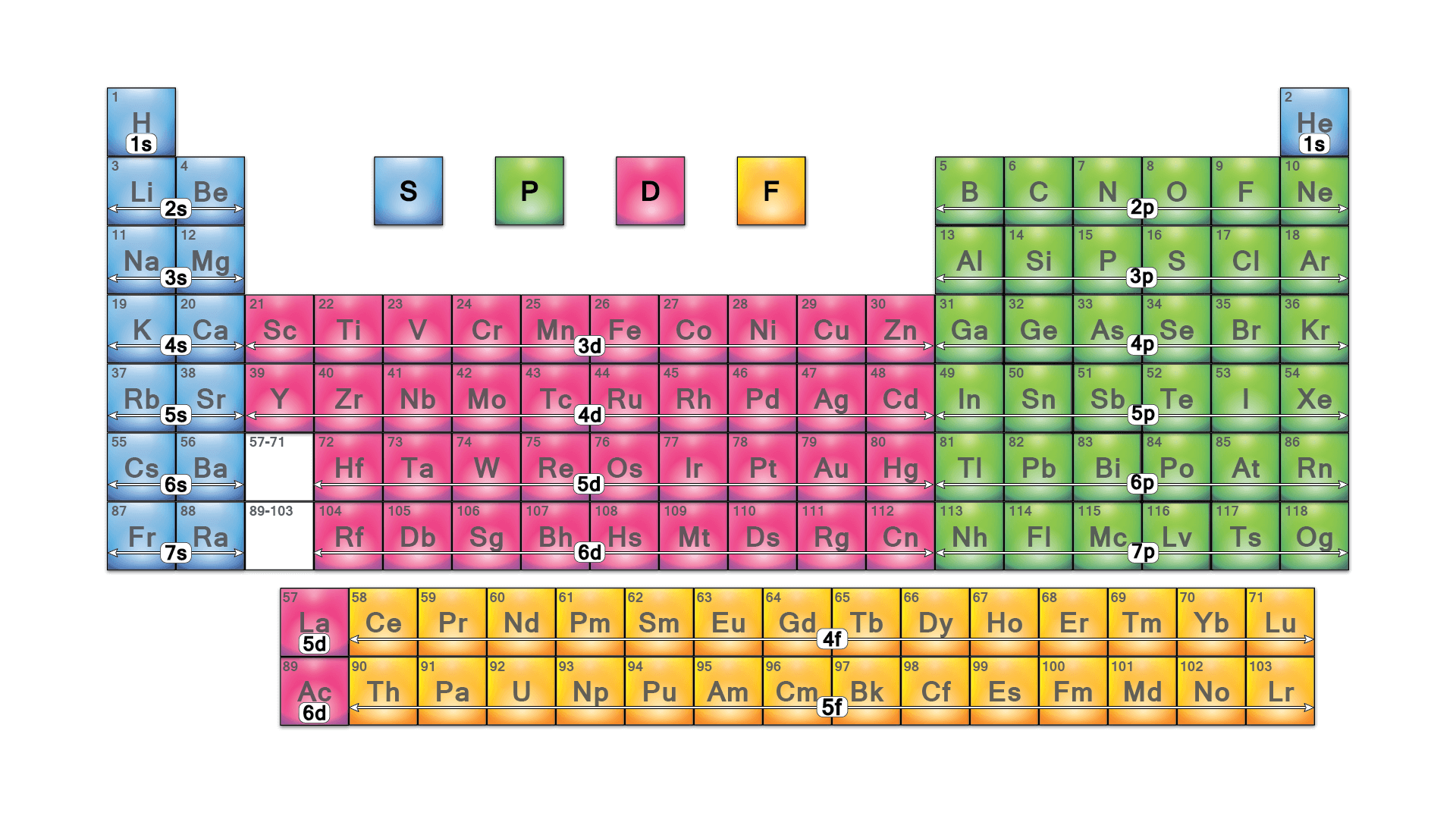
La tabla periódica es una herramienta fundamental en el estudio de la química y la comprensión de los elementos que componen nuestro mundo. Su estructura y organización nos permiten visualizar de manera ordenada y sistemática las propiedades de los elementos, así como su clasificación según su configuración electrónica. En este artículo, exploraremos en detalle los diferentes bloques que conforman la tabla periódica y cómo influyen en las propiedades de los elementos.
La tabla periódica es una disposición tabular de los elementos químicos, ordenados por su número atómico (número de protones en el núcleo) y distribuidos en filas llamadas periodos y columnas llamadas grupos. Esta herramienta es esencial para los químicos y científicos en general, ya que proporciona una visión sistemática de los elementos y sus propiedades.
Historia de la tabla periódica
La historia de la tabla periódica se remonta al siglo XIX, cuando los químicos comenzaron a darse cuenta de que existían patrones en las propiedades de los elementos. Figuras como Dmitri Mendeléyev y Julius Lothar Meyer jugaron un papel crucial en el desarrollo de la tabla periódica moderna, estableciendo las bases para su organización y clasificación.
Estructura y organización de la tabla periódica
La tabla periódica está organizada en siete periodos horizontales y dieciocho grupos verticales. Cada elemento está representado por un símbolo y su número atómico correspondiente. Además, la tabla periódica se divide en diferentes bloques, cada uno de los cuales tiene características particulares.
Propiedades periódicas de los elementos
Las propiedades periódicas son aquellas que varían de manera sistemática a medida que se avanza en la tabla periódica. Algunas de las propiedades periódicas más importantes incluyen el tamaño del átomo, la electronegatividad, la energía de ionización y la afinidad electrónica. Estas propiedades nos brindan información sobre las características y reactividad de los elementos.
Clasificación de los elementos en la tabla periódica
Los elementos en la tabla periódica se clasifican en diferentes categorías según sus características y propiedades. Estas categorías incluyen metales, no metales y metaloides. Cada categoría tiene propiedades específicas que los distinguen y nos permiten comprender mejor su comportamiento químico.
Aplicaciones de la tabla periódica en la vida cotidiana
La tabla periódica tiene numerosas aplicaciones en nuestra vida cotidiana. Desde la creación de materiales y compuestos químicos hasta la comprensión de los procesos biológicos, la tabla periódica es una herramienta esencial en la ciencia y la tecnología. También nos permite entender la composición de los alimentos, los medicamentos y otros productos que utilizamos a diario.
Conclusión
La tabla periódica es una herramienta invaluable en el estudio de la química y la comprensión de los elementos. Su estructura y organización nos permiten visualizar de manera ordenada y sistemática las propiedades de los elementos, así como su clasificación en diferentes bloques. Conocer los bloques de la tabla periódica nos ayuda a comprender las propiedades y reactividad de los elementos, y nos permite utilizar esta información en diversas aplicaciones en nuestra vida cotidiana.
Preguntas frecuentes
¿Cuántos bloques conforman la tabla periódica?
La tabla periódica se divide en cuatro bloques principales: el bloque s, el bloque p, el bloque d y el bloque f. Cada bloque tiene sus propias características y propiedades que influyen en el comportamiento de los elementos.
¿Cuál es el elemento más pesado de la tabla periódica?
El elemento más pesado de la tabla periódica es el oganesón (Og), con un número atómico de 118. Fue descubierto en 2002 y es un elemento superpesado y altamente radioactivo.
¿Cuál es el elemento más ligero de la tabla periódica?
El elemento más ligero de la tabla periódica es el hidrógeno (H), con un número atómico de 1. Es el elemento más abundante en el universo y tiene propiedades únicas debido a su configuración electrónica.
¿Cuál es el elemento más reactivo de la tabla periódica?
El elemento más reactivo de la tabla periódica es el francio (Fr), con un número atómico de 87. Es un metal alcalino altamente reactivo y extremadamente escaso en la naturaleza.